高吸収型クルクミン:セラクルミンMDX
ウコンに含まれるクルクミンには、抗がん作用を含め様々な薬効が報告されています。しかし、クルクミンは水に溶けにくく、経口摂取してもほとんどが消化管粘膜から吸収されずに体外に排出されます。したがって、クルクミンの薬効を利用するためには、体内への吸収率(消化管吸収率)を高めることが最重要課題になっています。
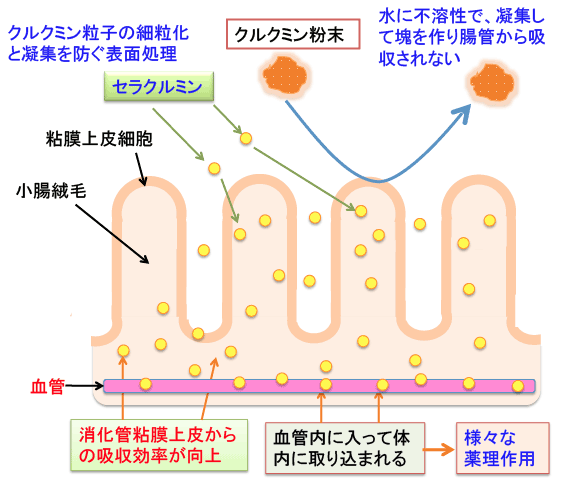
セラクルミン(Theracurmin)は、細粒化+表面処理技術によりクルクミンの消化管粘膜からの吸収率を大幅に高めた高吸収型クルクミンです。
|
|
|
従来のウコン粉末は水に溶けにくく消化管内で凝集して塊を作り、小腸粘膜からほとんど吸収されない。セラクルミンは粒子を非常に細かくし安定化させることによって、小腸粘膜からの吸収効率を高めている。
|
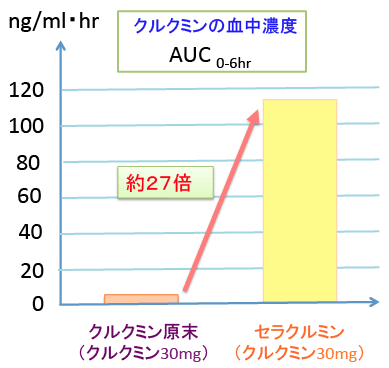
セラクルミンは消化管からの吸収率が高いため、同じ量のクルクミンを摂取しても、血中濃度は従来のクルクミンの約27倍になることが確認されている。
|
|
|
【セラクルミンMDX】
高吸収性クルクミン配合サプリメント
180カプセル入り(1カプセル当たりクルクミン30mg)
製造:株式会社セラバリューズ
価格:21,600 円(税込み)
クルクミン粒子を細粒化し、凝集を防ぐ表面処理を行うことによって、消化管粘膜からの吸収性を大幅に改善することに成功しました。通常のクルクミンに比べて血中濃度が約27倍になることが確認されています。
|
【服用法】
健康増進やがん予防の目的では1日1〜2カプセルを服用します。
がん治療の目的では、がんの進行状況や治療の状況に応じて、1日3〜9カプセルを目安に服用します。がん治療に併用する場合は、病状や治療状況を伺って服用法を決めますので、ご相談下さい。
ご希望の方あるいはご質問のある方はメール(info@f-gtc.or.jp)か電話(03-5550-3552)でお問い合わせください。

【クルクミンとは】
クルクミン(Curcumin)はウコンに含まれる成分の一つです。鮮やかな黄色を持つことから天然の食用色素として利用されています。最近はその健康作用が注目され、ドリンク剤や健康食品としても利用されています。
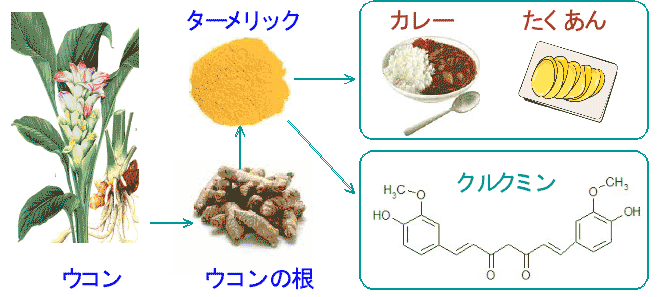
ウコン(Curcuma longa)はショウガ科の植物で、インドや東南アジアなどの熱帯地方、国内では沖縄・九州南部・屋久島に自生し、また栽培もされています。その根の部分は生姜に似ており、その乾燥粉末は「ターメリック」という香辛料であり、カレー粉の黄色い色素の元でもあるので馴染み深い食材です。黄色色素を利用してたくわんの着色剤やウコン染めの名で染料としても使われています。脂質の酸化を防ぐ作用があるため、食品の酸化防止剤としても利用されています。ウコンの粉末(ターメリック)には3〜5%程度のクルクミンが含まれています。(下図)
ウコンは古代インド医学(アーユルヴェーダ)から伝わった薬草で、胃腸病や炎症性疾患の治療に古くから用いられています。多くの国で民間薬としても使われています。漢方医学では、利胆(胆汁の分泌促進)、芳香性健胃薬の他に止血や鎮痛を目的に漢方処方に配合されます。
インドのアーユルヴェーダ医学では抗炎症作用が利用され様々な疾患の治療に用いられています。薬理作用としては、肝臓の解毒機能亢進作用、利胆作用、芳香健胃作用があります。抗動脈硬化作用、アルコール性肝障害の改善作用なども報告されています。
お酒を飲んだらウコンとよく言われますが、普段からウコンを摂取することで肝機能を丈夫にできます。ウコンに含まれるクルクミンは胆汁の分泌を促進する作用があり、肝臓における毒物の排泄を促進するからです。最近では、胃腸病や高血圧などの幅広い効用も認められるようになりました。民間療法や健康食品としてもポピュラーな食品です。
日頃からカレーを多く食べている人ほど、アルツハイマー病のような認知症の発症率や程度が低いという疫学研究の結果も報告されています。抗炎症作用や抗酸化作用が、脳の神経障害を防ぐ効果があるためと考えられています。
ウコンは血液循環を良くし、抗酸化作用と抗炎症作用が強く、抗がん作用もあるので、抗がん剤治療後の回復促進と再発予防にも効果が期待できるので、がんの漢方治療にもよく使用されています。
培養がん細胞を使った実験では、クルクミンおよびその類縁物質には、抗炎症、抗酸化、転写因子NF-κB の活性化阻害、誘導性一酸化窒素合成酵素(iNOS)やシクロオキシゲナーゼ-2(COX-2)活性阻害、がん細胞のアポトーシス誘導などの作用が報告されています。
 【クルクミンの抗炎症作用と抗がん作用】
【クルクミンの抗炎症作用と抗がん作用】
クルクミンは、強い抗酸化作用と同時に、NF-κBという転写因子の活性化を阻害することにより、炎症や発がんを促進する誘導性一酸化窒素合成酵素(iNOS)やシクロオキシゲナーゼー2(COX-2)の合成を抑えてがんの発生を予防したり、がん細胞を死にやすくするなどの効果が明らかにされ、がん予防物質として注目を集めています。
転写因子のNF-κB (Nuclear Factor-kappa B)は、通常は細胞内でIκB (Inhibitor of kappa B)という阻害蛋白と結合して不活性な状態で存在しています。マクロファージに炎症性のシグナルが来ると、IκB蛋白が分解してNF-κBはフリーになって細胞の核に移行します。核内においてiNOSやCOX-2などの遺伝子の調節領域に結合して、これらの蛋白質の合成を開始します。最近の研究で、クルクミンはIκBの分解を阻止してNF-κBの活性化を抑制することによって、マクロファージからのiNOSやCOX-2の合成を抑える作用機序が報告されています。
また、がん細胞においては、活性酸素などによってNF-κBが活性化されると、増殖が促進され、アポトーシスという細胞死が起こりにくくなります。アポトーシスとは、細胞がある情報を受けて、自ら能動的に死んでいく「プログラムされた細胞死」のことをいいます。多くのがん細胞は、転写因子NF-κBが活性化されるとアポトーシスが起こりにくくなって増殖速度が早くなります。がん細胞で活性化されたNF-κBを阻害してやるとがん細胞が抗がん剤で死にやすくなり、抗がん剤が効きやすくなります。クルクミンががん細胞のNF-κBの活性化を阻害してがん細胞のアポトーシスを引き起こすこと、抗がん剤感受性を高めることなどが報告されています。
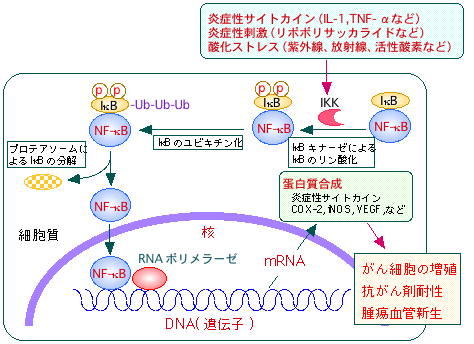 |
図:NF-κBは細胞質に存在し、IκBと呼ばれる制御蛋白質と複合体を形成している。炎症性刺激や酸化ストレスはIκBキナーゼ(IKK)を活性化してIκBをリン酸化し、さらにユビキチンが結合してプロテアソームで分解される。IκBが外れるとNF-κB分子内の核内移行シグナルが露出してNF-κBは核に移行し、目的遺伝子の転写を行う。がん細胞内でNF-κBが活性化されると、抗がん剤に対して抵抗性になり、増殖や転移が促進される。したがって、NF-κBの活性化を阻害すると、がん細胞の増殖を抑制し、抗がん剤感受性を高めることができる。 |
動物発がん実験や移植腫瘍を用いた研究で、クルクミンの発がん予防効果や腫瘍縮小効果などが報告されています。1988年、アメリカのラトガ−ス大学薬学部のコニー博士らは、マウスを使った実験を行い、クルクミン皮膚がんの発生を抑制するという研究結果を報告しました。それ以来、日本や台湾を中心にウコンのがん予防効果の研究が進められています。発がん物質を使った動物実験では、皮膚がん、胃がん、大腸がん、乳がん、肝臓がんなどの発生を抑える効果が報告されています。
培養細胞を使って実験レベルですが、クルクミンとCOX-2阻害剤のセレコキシブ(celecoxib)を併用すると結腸直腸がんの増殖を相乗的に阻害したという報告があります。肝臓がんや卵巣がんなどのがん細胞に対するシスプラチン、ドキソルビシン、タキソールの抗がん作用をクルクミンが増強したという報告もあります。クルクミンのがん予防効果や、がん患者における抗腫瘍効果を検討する多数の臨床試験が米国などで実施されています。
 【クルクミンは放射線治療の副作用を弱め抗腫瘍効果を高める】
【クルクミンは放射線治療の副作用を弱め抗腫瘍効果を高める】
放射線治療はがん細胞を殺すために行うのですが、放射線照射は活性酸素を発生させるので正常組織のDNAも傷つけて別のがんが発生したり、残っているがん細胞を悪化させたりする可能性もあります。放射線自体に発がん性があることはよく知られています。マウスやラットに放射線を当てて皮膚がんや乳がんを作る実験モデルにおいて、クルクミンが放射線による発がんを予防することが多く報告されています。
また、放射線照射による酸化ストレスによって、前述のようにNF-κBの活性化が起こると、がん細胞はアポトーシスを起こしにくくなって放射線治療に抵抗するようになります。つまり、がん細胞に放射線を照射していると、次第に放射線が効きにくくなるのです。放射線の殺細胞効果に対してがん細胞が抵抗性を獲得することをクルクミンが予防する実験結果も報告されています。クルクミンはがん細胞に直接アポトーシスを引き起こす作用も報告されていますので、放射線治療中にクルクミンを摂取することは、抗腫瘍効果を高めることになります。
クルクミンが放射線の発がんを予防し、放射線の抗がん活性を高める効果が実験で報告されていますので、乳がんなどで放射線治療を行うときにクルクミンを併用すると、治療効果を高めると同時に、再発を予防する効果も期待できそうです。
 【クルクミンはがん細胞に対する免疫寛容を軽減する可能性が報告されている】
【クルクミンはがん細胞に対する免疫寛容を軽減する可能性が報告されている】
ウコンあるいはクルクミンの免疫力に対する研究報告は、今まで免疫細胞のNF-κB活性を阻害する作用があるため、免疫力を弱める可能性の方が指摘されていました。つまり、マクロファージやリンパ球などの免疫細胞のNF-κB活性を阻害すると、炎症性サイトカインのTNF, IL-1, IL-2, IL-6, IL-8, IL-12, などの発現を低下させるためです。
このような炎症性サイトカインの発現を抑制することがウコンやクルクミンの抗炎症作用や発がん予防効果の作用機序の一つと考えられていますが、これらの炎症性サイトカインの抑制は免疫力を弱める結果になると考えられたからです。しかし、最近の研究では、がん細胞に対する免疫寛容の状態をクルクミンが軽減する効果が報告されています。
がん細胞は宿主細胞とは異なる抗原を有しているので、免疫学的には宿主の免疫細胞(T細胞やNK細胞)によって拒絶されるはずです。したがってがんが増殖や進展をするためには宿主免疫監視機構からの逃避(
免疫寛容)が必須であり、この免疫寛容の成立において重要な役割を果たす
インドールアミン酸素添加酵素の活性をクルクミンが阻害して抗腫瘍免疫を高めることが報告されています。
インドールアミン酸素添加酵素(Indoleamine 2,3-dioxygenase: IDO)は、アミノ酸のトリプトファンをN-Formylkynurenineへ代謝する酸素添加酵素で、ヒトの肺、小腸、胎盤など多くの組織に分布し、種々の感染症や炎症で強く誘導されます。
IDOは免疫システムにおいて重要な役割を担っており、特に、抗原提示細胞の樹状細胞のあるサブクラスに発現するIDOは抑制性T細 胞を誘導し免疫寛容(免疫抑制)の成立に関与します。
その作用機序は局所的なトリプトファンの枯渇とその代謝産物(キヌレニンなど)による阻害作用と考えられています。多くの癌ではIDOの高発現が認められ、がん細胞はその免疫抑制作用を巧みに利用して宿主の免疫監視機構を回避しつつ増殖していることが知られています。さらに、IDOを多く発現しているがん細胞が進行が早く、治療に抵抗して予後が悪いことが報告されています。
最近の報告で、ウコンに含まれる
クルクミンには、活性化した樹状細胞のインドールアミン酸素添加酵素を抑制して抗腫瘍免疫を高めることが報告されています。(J. Biol. Chem. 284:3700-3708, 2009)
慢性炎症は発がんを促進すると同時に、免疫抑制系のT細胞を活性化し、樹状細胞やキラーT細胞の活性を弱めることが知られています。したがって、抗炎症作用のあるクルクミンは、炎症に由来して抗腫瘍免疫を抑制している要因(IDOの活性上昇やCOX-2の発現上昇など)を阻害することによって、免疫寛容状態を軽減して、がん細胞に対する免疫力を高める効果が指摘されているのです。
NF-κBやIDO(インドールアミン酸素添加酵素)の活性やCOX-2の発現に対するクルクミンの阻害作用は、培養細胞を使った実験結果によるものが主で、その有効濃度は人間での血中濃度に比べて極めて高いので、人体内で本当にそのような効果が期待できるのかという疑問もあります。したがって、クルクミンの抗炎症作用が、抗腫瘍免疫の増強に対してプラスに働くのかマイナスに作用するのかは、今後の研究結果を待つ必要があります。しかし、最近の研究の流れは、クルクミンが免疫寛容を軽減して抗腫瘍免疫を高める可能性の方が注目されているようです。

図:慢性炎症は、転写因子NF-κBの活性を高めてがん細胞の増殖を促進すると同時に、抗原提示細胞(樹状細胞)のインドールアミン酸素添加酵素の活性を高めたり、シクロオクシゲナーゼ-2の活性化などによって、がん細胞に対する免疫寛容の成立に関わっている。クルクミンはがん細胞の増殖を抑えると同時に、免疫寛容を軽減する効果も期待できる。。
 【クルクミンの臨床試験】
【クルクミンの臨床試験】
培養細胞や動物を使った実験でクルクミンには様々な薬理作用が報告されていますが、問題はそのような効果が人間がクルクミンを摂取した場合でも起こりうるかどうかという点です。
クルクミンの腸管からの吸収率は極めて低く、血中の半減期が短いことが問題視されています。
例えば、ラットで500mg/kgのクルクミンを投与して血中濃度のピークは1.8ng/mlという報告があります。多くの実験でがん細胞の増殖を抑制する濃度はμg/mlのレベルですので、この結果は、人間が数グラムのクルクミンを摂取しても、がん細胞に何らかの影響を及ぼすことは考えにくいということになります。(1ngは1gの10億分の1、1μgは1gの100万分の1。つまり、1μg=1000ng)
人間での第1相試験で、8グラムのクルクミンを3ヶ月間服用して、血中のクルクミン濃度は1μM程度という報告もあります。
クルクミンは小腸粘膜と肝細胞で急速に代謝(glucuronidation, sulfatation)され、人間で2〜8gのクルクミンを摂取しても、血中濃度は検出できないレベルか、低レベル(0.51-1.77 micro M)という報告もあります。
以上のことから、臨床試験で有効性が証明されないと、クルクミンのサプリメントとしての摂取が有用とは評価できません。この点については、まだ結論が出ていませんが、以下のような臨床試験の報告があります。
| ○関節リュウマチ患者を対象にした臨床試験では、クルクミン(1200mg/日)はピラゾロン系抗炎症薬のフェニルブタゾンに匹敵する抗炎症作用を示し、副作用は極めて少ないことが報告されている。 |
| ○がんのハイリスクグループ(前がん病変がある患者)に投与してがん予防効果が示唆されている。 クルクミンを1日500mgから初めて8gまで増量しながら3ヶ月投与。 子宮頸部の異型上皮、胃の腸上皮化生(intestinal metaplasia of the stomach)や膀胱の異型上皮(膀胱がん切除後)、口腔の白班(leukoplakia)、皮膚のBowen病などの前がん病変の患者25例中7例で、前がん病変の組織学的な改善を認めた。(Anticancer Res 2001, 21:2895-2900) |
○Phase II trial of curcumin in patients with advanced pancreatic cancer.(進行膵臓がん患者に対するクルクミンの第2相試験) Clin Cancer Res. 14:4491-4499, 2008
米国のテキサス大学のMDアンダーソンがんセンターからの報告。 進行した膵臓がん患者に1日8gのクルクミンを投与して、がんの進行や、血中のサイトカインの量、血液中の単核球のNF-κBやCOX-2の活性などに対する効果を検討。 投与した25人のうち21人がその反応を評価できた。
血中のクルクミンはグルクロン酸や硫化物が結合した代謝産物として検出されたが、その濃度は低く、経口摂取での吸収率が悪いことが示唆された。
2例において臨床的効果が認められた。1例は18ヶ月以上に渡り、腫瘍が増大しない状態が継続している。もう1例は、短期間ではあったが、73%の腫瘍の縮小を認めた。副作用は認めなかった。
血中の単核球のNF-κBやCOX-2などの炎症性シグナルは膵臓がん患者では正常よりも高いが、クルクミン投与によりこれらの炎症性シグナルに活性が低下していた。 血中のクルクミンのピークの濃度は22〜41ng/mlで、患者間のばらつきが大きかった。
(結論) クルクミンの経口摂取による消化管からの吸収は低いが、副作用はなく、一部の進行膵臓がん患者では、臨床的な抗腫瘍効果が認められた。
(注)この報告に対して、クルクミンを1日8gの投与で血中濃度は 22-41 ng/mLにしか達しないのに、なぜ効果がでるのかという疑問の意見もある。 クルクミンの分解産物のferulic acid と vanillinが効いているという推測もある。 |
| ○大腸がん患者15例にウコンエキスを1日440〜2200mg(クルクミンに換算して36から180mgの低用量)を4ヶ月間投与。 腫瘍マーカーの低下が1例、CT上の腫瘍不変(stable disease)が5例に認められた。(Clin Cancer Res, 2001, 7:1894-1900) |
| ○クルクミンの大量投与(900〜3600mg, 8000mgなど) で、進行大腸がん患者で腫瘍の増大が抑制(数ヶ月のstable disease)。ただし、服用量が多くなると下痢などの副作用が出る。 (Clin Cancer Res 2004, 10:6847-6854) |
| ○家族性大腸ポリポーシスの患者5人に対してクルクミン450mg+ケルセチン20mgを1日3回、6ヶ月間の投与で5人全ての患者で効果がみられ、ポリープの数(平均減少率60.4%)とサイズ(平均減少率50.9%)のどちらも統計的に有意な減少であった。 |
現在、様々ながんでクルクミンの抗腫瘍作用に関する臨床試験が進行中です。クルクミン単独、あるいは抗がん剤など他の治療との併用効果が検討されています。多くの研究者がクルクミンの抗がん作用に注目して研究しているのは確かです。
がん予防効果や、進行膵臓がんに対する有効性を示唆する報告などがあります。しかし、クルクミンは腸管からの吸収率が低く、体内での半減期も極めて短いので、その有用性については疑問点が多いのも事実です。現時点での臨床試験の結果からは1日8g程度のクルクミンを服用しないと抗腫瘍効果が期待できそうも無いので、サプリメントとしてがん治療に使うには問題があります。生体利用性(バイオアベイラビリティ)を高めたクルクミン製剤やクルクミン誘導体の開発などが行なわれており、そのような製品が開発されれば、有用性が高まる可能性はあります。
 【生物学的利用能(バイオアベイラビリティ:bioavailability)とは】
【生物学的利用能(バイオアベイラビリティ:bioavailability)とは】
培養細胞や動物を使った基礎研究では、クルクミンががんや循環器疾患や神経変性疾患など様々な病気の予防や治療に効果が期待できることが示唆されています。しかし、これらの薬効が人間の病気に有効かどうかはまだ十分な証拠はありません。
クルクミンを服用しても、あまり効果が期待できないという意見があります。効果を期待するためには、かなり大量のクルクミンを服用する必要があると考えられています。その理由は、クルクミンは腸管からの吸収が極めて悪いためです。クルクミンは水に溶けにくいため、そのまま服用しても、消化管内で凝集し、ほとんど体内に吸収されないことが知られています。
薬学の分野では「生物学的利用能(バイオアベイラビリティ:bioavailability)」という用語があります。投与された薬物の何パーセントが血中に入って体に作用するかを表す指標です。薬を静脈内に投与すると、投与された薬物はほぼ完全に生体で利用されるので、バイオアベイラビリティは100%ということになります。一方、口から摂取(経口投与)した場合は、薬剤の消化管からの吸収の程度によってバイオアベイラビリティは影響を受けます。腸管からの吸収が悪いとバイオアベイラビリティの数値は極端に低くなります。一般的に、水に溶けにくい成分(高脂溶性の化合物)は消化管粘膜からの吸収性が悪いことが知られています。内服薬の場合、バイオアベイラビリティが十分に高い医薬品を創製できるかどうかが医薬品として成功するかどうかを決定する最も重要な要因の一つであるとされています。
通常のクルクミンは水に溶けにくく、そのまま服用しても消化管内で凝集し、体内にほとんど吸収されないことが明らかになっています。通常のクルクミンのバイオアベイラビリティは0.1%以下で、ほとんどが便と一緒に体外に排出され、体内では利用されていないことが明らかになっています。
したがって、基礎研究で明らかになっているクルクミンの薬効を人間で利用するためには、クルクミンのバイオアベイラビリティを高めること、すなわち消化管粘膜からの吸収を高めることが最も重要だと言えます。
薬剤のバイオアベイラビリティを高める製剤技術が開発され、サプリメントの分野でも、体内吸収性を高めた製品の開発が行われています。例えば、当クリニックで推奨しているシクロカプセル化CoQ10やシクロカプセル化R体αリポ酸は、γ-シクロデキストリンを用いて、高脂溶性のCoQ10やR体αリポ酸のバイオアベイラビリティを高めることに成功した製品です。
クルクミンに関しても、消化管からの吸収を高めて生物学的利用能を改善した製品が開発されています。その一つがセラクルミンです。